细说医疗器械注册人制度下的CDMO新模式



文文

达达,广东和天津的医疗器械注册人在8月16日也正式获得批复,之前我认真看了上海注册人制度相关文件,总算是有点头绪了。

文文

最近经常看到一个CDMO模式,感觉大家都非常关注。奥咨达作为国内领先的CDMO+CRO平台,能否解释下CDMO呢?
达达
CDMO是一种新兴外包服务模式。为注册申请人提供创新性的研发转化及规模化生产服务,以附加值较高的技术输出取代单纯的产能输出。



文文

那CDMO模式与现在传统的医疗器械模式相比较有何优势?
达达
注册人制度的开放使得国内注册申请人可以免去自建厂房、购买设备、体系建设等前期工作,委托有资质的生产企业生产样品及量产。一般而言,除产品研发时间,医疗器械产品上市耗时至少3-8年。以国内二类生产企业三年时间为例(如下图),时间与经营成本投入巨大,同时面临着合规合法的高风险与试错成本。
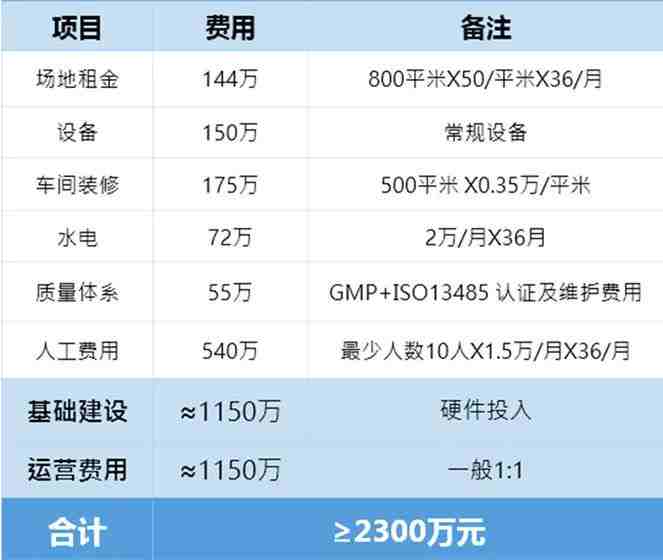
而奥咨达CDMO+CRO平台针对注册申请人困局,价值在于:




文文

具体的CDMO合作流程如何呢,在合作过程中双方的职责分别有哪些?
达达
CDMO模式是以合同的形式开展合作,双方需签订相关的委托合作协议等,奥咨达CDMO合作流程可见下图。




文文

注册人制度下,委托方在实际操作过程中如何管控受托方的产品质量?
达达
首先注册人制度下要求注册申请人在工商注册时必须配备专职的法规事务、质量管理、上市后事务等相关人员,拥有相应的专业背景和工作经验且不得互相兼职,具备医疗器械全生命周期管理能力,有对质量管理体系进行评估、审核和监督的人员条件;
第二在委托时必须选择符合委托产品要求的生产体系与代工能力的生产企业;
第三,委托生产时,在合同中体现受托方需保证生产资料做到真实、完整、可追溯,定期进行核查。



文文

感谢达达为我解惑,对于CDMO又学到了新知识,这回能够跟上咱们医疗器械产业发展的脚步了!
达达
应该的。奥咨达作为CDMO+CRO平台服务生,聚集资本+技术+法规+产业,加速医疗器械产业发展,也很欢迎医械人的多多咨询讨论。欢迎随时交流哦!




热点推荐
可点击标题阅读原文
最新评论
推荐文章
作者最新文章
你可能感兴趣的文章
Copyright Disclaimer: The copyright of contents (including texts, images, videos and audios) posted above belong to the User who shared or the third-party website which the User shared from. If you found your copyright have been infringed, please send a DMCA takedown notice to [email protected]. For more detail of the source, please click on the button "Read Original Post" below. For other communications, please send to [email protected].
版权声明:以上内容为用户推荐收藏至CareerEngine平台,其内容(含文字、图片、视频、音频等)及知识版权均属用户或用户转发自的第三方网站,如涉嫌侵权,请通知[email protected]进行信息删除。如需查看信息来源,请点击“查看原文”。如需洽谈其它事宜,请联系[email protected]。
版权声明:以上内容为用户推荐收藏至CareerEngine平台,其内容(含文字、图片、视频、音频等)及知识版权均属用户或用户转发自的第三方网站,如涉嫌侵权,请通知[email protected]进行信息删除。如需查看信息来源,请点击“查看原文”。如需洽谈其它事宜,请联系[email protected]。
