谷歌领投 1.07 亿美元助力 CD73 抗体药物研发


文/方信
编/Ginger, HLR
2007 投资 23andMe 后 10 余年来, 谷歌一直在积极进行着进军医疗行业的布局。2017 年 11 月,谷歌斥资 1.07 亿美元领投了一家名为 Arcus Biosciences 的生物技术创新公司。这家 2015 年才成立的公司迄今为止已进入 C 轮融资,总融资额高达 2.26 亿。
而药明生物和誉衡药业也将 PD-1 抗体 GLS-010 的国际权益授权给 Arcus Biosciences。那么它是凭借什么让包括谷歌在内的投资人及医药公司信心满满?
Arcus 的主打产品之一就是针对本文关注靶点 CD73 的名为 AB690 的单克隆抗体药物。除 Arcus 之外,还有老牌大型医药公司,比如 Bristol-Myers Squibb (BMS)也在有条不紊地进行着靶向 CD73 的研发,并且还作为唯一的外国机构在中国申请了 CD73 抗体在肿瘤中应用的专利 (CN107001474A), 其雄心可见一斑。
在本次 ASCO 国际学术会议当中,共有五篇 CD73 相关研究,五篇研究均证实了 CD73 的高表达量与癌症发展的关系,以及 CD73 在癌症免疫治疗的重要作用。下文将对五篇摘要进行介绍。
1
CD73
CD73 是 NT5E 基因编码的胞外-5'-核苷酸酶,可将细胞外腺苷一磷酸(AMP)转化为腺苷(adenosine)的关键酶。腺苷与腺苷受体 A2AR(adenosine receptor AR)结合可抑制 T 细胞的免疫作用,进而帮助癌细胞逃逸 T 细胞的“追杀”。
CD73 在多种肿瘤当中都过量表达,除了抑制免疫细胞功能,越来越多的研究表明 CD73 也可以直接刺激肿瘤细胞增殖,迁移和侵袭,及肿瘤血管生成。由此可见,CD73 和其他调节免疫应答的靶点比较,有着一箭双雕的优势。
去年,Cell 子刊《Trends in Cancer》发表了“Anti-CD73 in Cancer Immunotherapy: Awakening New Opportunities”。文章系统讨论了 CD73 与肿瘤发生、发展以及扩散之间的关系,如下图所示。尽管第一代针对 PD-(L)1免疫检查点抑制剂的开发使癌症免疫治疗进入了一个新时代,但科学家们也在积极研究其它的检查点通路。文章强调了 CD73 在驱动癌症免疫逃逸中发挥了关键的作用,说明这一分子作为癌症治疗潜在靶点的药物价值。并且临床前研究表明,靶向 CD73 能够产生良好的抗肿瘤作用,且将 CD73 阻断治疗与其它免疫分子调节剂联合(如PD-(L)1抗体)是极具吸引力的选择。
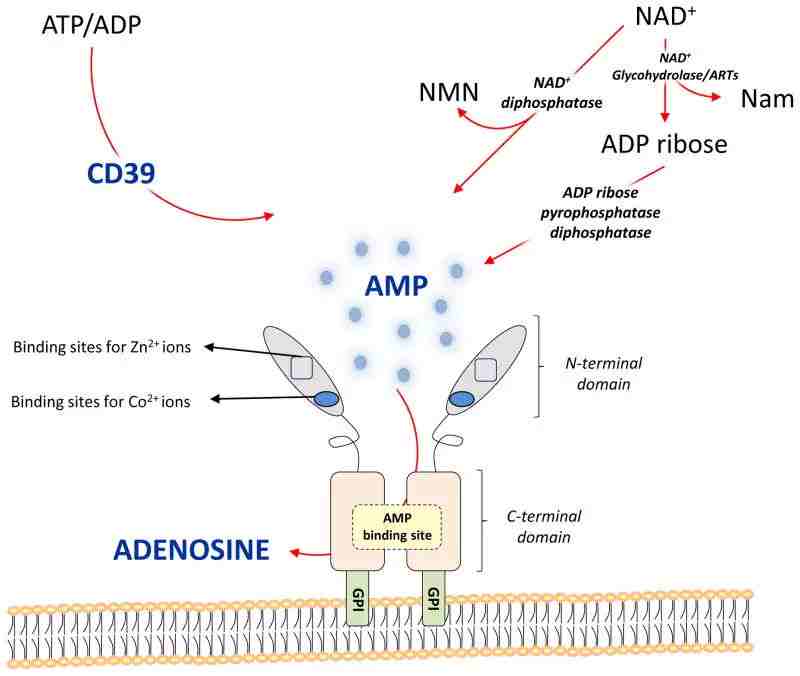
▲ CD73 胞外作用机制
2
CD73 @ ASCO 2018
1. CD73 在结直肠癌肝转移中的预后作用。(摘要号3584)
本实验对从 214 例患者(2011-2014)切除的 391 例大肠癌肝转移(CRLM)样品进行组织芯片的分析,并随访病人预后状况至 2017 年 10 月。通过多变量分析,CD73 表达量高的 CRLMs 组普遍具有不良预后结果,实验结果不受限于复发时间(time to recurrence,TTR)和特异性生存期(disease specific survival,DSS)临床病理特征。
结论:此研究证实 CD73 在 CRLMs 中的表达可帮助识别部分全身化疗后预后不良的患者,从而为研究 CD73 抗体或腺苷 A2A 受体抑制剂的临床实验提供指导。
2. CD73 表达在接受免疫检查点抑制剂的 EGFR 突变阳性非小细胞肺癌(non-small cell lung cancer,NSCLC)患者的预测作用。(摘要号9065)
实验筛选了接受了完全切除的处于 I-III 期 EGFR 突变阳性的非小细胞肺癌患者(队列 A,67 例),接受了 EGFR-TKI 治疗的晚期非小细胞肺癌或复发非小细胞肺癌患者(队列 B,17 例)以及耐药后使用免疫检查点抑制剂治疗的 EGFR 突变阴性非小细胞肺癌患者(31 例)。通过免疫组化分析来评估 CD73 的表达量,在 50% 以上的肿瘤细胞中存在 CD73 染色的肿瘤被评为 CD73 高表达。
结论:CD73 的表达可帮助预测 EGFR 突变阳性非小细胞肺癌患者接受免疫检查点抑制剂预后情况。
3. 非小细胞肺癌中CD73表达的免疫学和临床意义。(摘要号12050)
本实验从癌症基因组图谱(The Cancer Genome Atlas,TCGA)获得 CD73 表达量数据, 样品包括肺腺癌(n = 517)和鳞状细胞癌(n = 501),根据 CD73 的 mRNA 表达水平(低,中等,中高,高)对样品进行分组。在 CD73 高表达组(CD73-H)和 CD73 低表达组(CD73-L)之间进行免疫情况对比,包括免疫细胞浸润,免疫检查点和细胞因子,肿瘤突变负荷(tumor mutation burden,TMB),新抗原负荷和存活结果。
结论:通过超过 1,000 人类肺癌样品的分析,本实验首次报道了 CD73 表达与活化的 CD4 和 CD8 T 细胞的肿瘤浸润之间的反向关联。此外,与 CD73 低表达组相比,CD73 高表达组显示不利生存。
4. MEDI9447(Oleclumab)单独使用或联合Durvalumab用于治疗晚期结直肠癌(colorectal cancer,CRC)或胰腺癌(pancreatic cancer)的安全性,有效性和药效学(PD)。(摘要号4123)
实验病人接受 3 + 3 剂量递增实验设计,接受 4 种递增剂量的 Oleclumab IV 中的一个,伴随或不伴随静脉注射 Durvalumab( 10mg / kg)每两周一次,直至疾病进展,随后用高剂量 Oleclumab 加 Durvalumab 10mg /千克,每两周一次。Oleclumab 和 Durvalumab 治疗具有可控的安全性和药效型与药物作用机制一致。
结论: 在胰腺癌和晚期结肠癌患者的联合疗法中显示早期积极药效。(临床试验信息:NCT02503774)
5.抗 PD1(muDX 400)疗法对辐射后的(CD8 + Tim3-CD73 +)干细胞样细胞有巨大影响:对改进包含辐射和抗 PD1 的临床试验设计的影响。(摘要号e21525)
实验使用人类等效同基因小鼠模型在 B16F10 GP 两侧植入了 B16 黑素瘤细胞,并使用不同剂量的辐射。对于免疫疗法,则使用 PD1 抗体(muDX400)。
结论: 结合放疗与抗 PD1 抗体的治疗将产生持续的远隔反应,并对干细胞样细胞产生巨大影响,使其产生更多效应细胞。这项研究将为临床试验设计中优化针对辐射和抗 PD1 疗法的最佳辐射剂量和测序改进提供一个平台。
3
结言
CD73 的临床实验相对较少,其中 4 个临床试验处于一期招募阶段,包括单药以及与 A2AR、PD-L1 (MEDI4736) 抑制剂的联合用药; 2 个临床实验一期完成进入 2 期招募阶段。
CD73临床实验 | 数量 |
一期 | 4 |
一期/二期联合 | 2 |
总数 | 6 |
CD73 是否能够不负众望,成为肿瘤免疫疗法的“明日之星”?Arcus 除了 CD73,又有哪些别的管线?答案都在我们即将推出的 “PD-(L)1联合疗法专题”,不见不散。
参考资料:
- PD-(L)1联合疗法专题
- Gao, Z.W., K. Dong, and H.Z. Zhang, The roles of CD73 in cancer. Biomed Res Int, 2014. 2014: p. 460654.
- Antonioli, L., et al., Anti-CD73 in cancer immunotherapy: awakening new opportunities. Trends Cancer, 2016. 2(2): p. 95-109.
- Corvus制药公司简介. Available from: https://www.pharmacodia.com/yaodu/html/v1/approve/1e130abf6523af39c94d7d736db26a7c.html.
- Google也投资癌症免疫疗法!领投生技新创Arucs1.07亿美元. 2017; Available from: http://www.genetinfo.com/investment/featured/item/12565.html.


本期作者:方信
2016 年毕业于南京农业大学,专业为动物医学。现于美国德州农工大学(Texas A&M University)攻读博士学位,专业为动物医药,从事生殖癌症方向的研究。现任美柏医健研究员。
ASCO 靶点解读专题
美柏路演
▼ 点击阅读原文,查看更多好内容
阅读原文 最新评论
推荐文章
作者最新文章
你可能感兴趣的文章
Copyright Disclaimer: The copyright of contents (including texts, images, videos and audios) posted above belong to the User who shared or the third-party website which the User shared from. If you found your copyright have been infringed, please send a DMCA takedown notice to [email protected]. For more detail of the source, please click on the button "Read Original Post" below. For other communications, please send to [email protected].
版权声明:以上内容为用户推荐收藏至CareerEngine平台,其内容(含文字、图片、视频、音频等)及知识版权均属用户或用户转发自的第三方网站,如涉嫌侵权,请通知[email protected]进行信息删除。如需查看信息来源,请点击“查看原文”。如需洽谈其它事宜,请联系[email protected]。
版权声明:以上内容为用户推荐收藏至CareerEngine平台,其内容(含文字、图片、视频、音频等)及知识版权均属用户或用户转发自的第三方网站,如涉嫌侵权,请通知[email protected]进行信息删除。如需查看信息来源,请点击“查看原文”。如需洽谈其它事宜,请联系[email protected]。