ASCO 2018 摘要靶点深度解读专题——KIR
平均阅读时长为 2分钟


文/Echo 徐
编/Ginger, HLR
肿瘤免疫疗法中,如果说 T 细胞是元老级成员,那么自然杀伤细胞(NK 细胞)可称得上是一颗冉冉升起的新星了,其在免疫系统对抗肿瘤中的作用得到越来越多的关注和研究。然而,中国药企对这个新型的领域的开发基本处在空白期。
即将拉开帷幕的 2018 ASCO 年会也带来了关于 NK 细胞免疫疗法的新动向。作为美柏医健 ASCO 2018 年会摘要深度解析的一部分,本文笔者带大家梳理以 NK 细胞 KIR 为靶点的新进展。
1
NK 细胞,KIR 与肿瘤免疫疗法
人体的免疫系统由两大部分组成:先天性免疫系统(Innate Immunity)与获得性免疫系统(Adaptive Immunity)。T 细胞是获得性免疫系统的重要组成部分,由于其既具有细胞杀伤作用,又能够对抗原产生记忆,在肿瘤免疫疗法中得到了最多的关注。然而,作为先天性免疫系统中的另一员大将,NK 细胞同样具有强大的肿瘤杀伤功能,近些年也开始得到器重。
与 T 细胞相似,正常生理状态下,NK 细胞处于“静息”状态。Killer cell immunoglobulin like receptor (KIR) 就是 NK 细胞表面一类可以调节 NK 细胞活性的受体,其中 KIR2DL1/2/3、KIR3DL1/2/3 属于抑制性受体。肿瘤细胞“聪明地”利用了这一机制,发动 HLA(Human Leukocyte Antigen)“部队”与这些抑制性受体结合,抑制 NK 细胞对其识别和杀伤。阻断肿瘤细胞 HLA 与 NK 细胞抑制性 KIR 受体之间的相互作用,为 NK 细胞免疫检查点抑制疗法提供了理论依据。
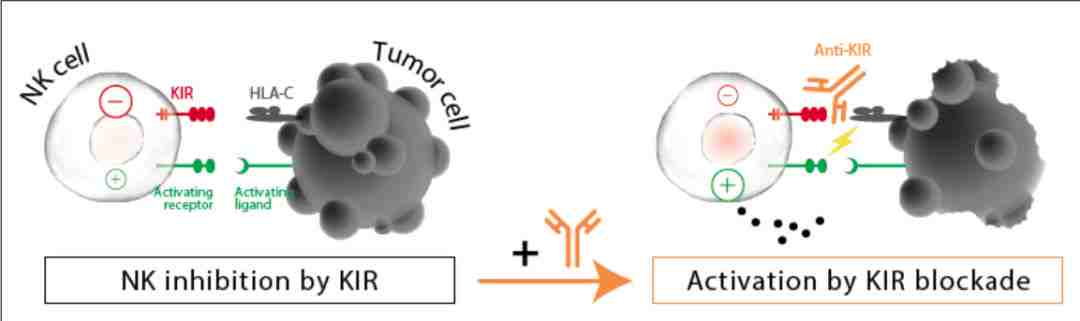
▲ 图片来源:Innate Pharma
目前,医药市场上,以 KIR 为靶点的研究处于 Innate Pharma 一家独大的局面,该公司于 1999 年由六位先天性免疫系统研究专家成立,发展势头迅猛。BMS 更是在 2011 年以 $465M 的价格获得了其靶向 KIR2DL1/2/3 的单抗产品 Lirilumab (IPH2102/BMS-986015)的独家开发、生产、销售权。目前,Lirilumab 有多项单用(NCT01687387),与 CTLA4(NCT01750580);PD1(NCT01714739、 NCT03203876); 5-azacytidine(NCT02399917、NCT02599649);Rituximab(NCT02481297); Elotuzumab(NCT02252263) 联用的试验处于临床 1/2 期研究阶段。此外,Innate Pharma 靶向 KIR3DL2 的同类第一的单抗产品 IPH4102 也已进入临床阶段(NCT02593045)。
Lirilumab 相关的临床试验中,最受瞩目的是其单用作为老年急性淋巴细胞白血病维持治疗(EFFIKIR,NCT01687387)的试验,以及与 anti-PD1 纳武单抗联用治疗多种肿瘤的试验(NCT01714739)。关于 Innate Pharma 及其产品临床试验的详细分析敬请关注美柏针对 KIR 靶点的深度分析系列文章。那么,ASCO 2018带来了哪些关于KIR的新消息呢,下面为大家一一盘点。
2
KIR @ ASCO 2018
1.anti-KIR 作为免疫检查点抑制疗法,提高化疗效用(摘要号:6015)
虽然部分肿瘤患者在接受了免疫检查点抑制剂(ICI,Immune checkpoint inhibitors)治疗之后,仍然发生了疾病进展,已有大量研究表明,在非小细胞肺癌患者中,该轮免疫疗法提高了接下来进行的补救性化疗(SCT,salvage chemotherapy)的治疗效果。
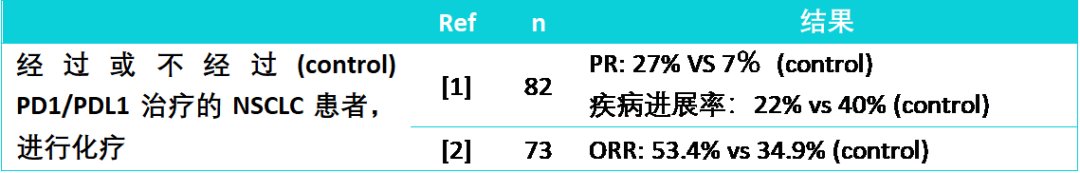
复发性/转移性鳞状细胞头颈癌患者对 ICI 的总体响应率(ORR,overall response rate)在 13-17%。
一项在法国进行的回顾性研究,分析了经 ICI 治疗后疾病发生进展,随后在 2014 年 9 月到 2018 年 1 月接受 SCT 的 84 位 R/M SCCHN 患者[3]。这 84 位患者经历过 anti-PD1, anti-PD-L1, anti-CTLA4 或 anti-KIR 治疗,疾病进展后接受紫杉醇类(56%)、铂类(37%)或甲氨蝶呤(7%)化疗。
分析结果表明:患者对 SCT 的 ORR 为 30%,3 位(4%)患者产生完全响应,22 位(27%)患者产生部分响应,疾病控制率为 57%。与单用化疗药相比,预先 ICI 治疗提高了 SCT 的治疗效果。
若按照患者接受的免疫抑制剂进行分类,该研究将提供与经典免疫抑制剂疗法(anti-PD1, anti-PD-L1, anti-CTLA4)相比,anti-KIR 的效用信息。
2.Lirilumab 临床试验新进展(摘要号:7067,临床试验号:NCT02599649)
2004 年,FDA 批准 Celgene 公司的 5-azacytidine(AZA),用于治疗骨髓异常增生综合征(MDS,myelodysplastic syndrome),尚未被批准用于治疗急性骨髓性白血病。AZA 通过促使 DNA 去甲基化,恢复调节细胞周期、分化的基因的正常功能。
早在 2015 年 4 月,BMS 与 MD 安德森癌症中心发起的 2 期试验(NCT02399917)研究 Lirilumab 与 AZA 联合治疗难治性/复发性急性骨髓性白血病患者的安全性和耐受性,截至目前,试验结果表明,治疗后复发的 AML 患者对 AZA 完全剂量与 Lirilumab 联合应用耐受良好。
2016 年 3 月,BMS 与 MD 安德森癌症中心又发起了另外一项 2 期试验( NCT02599649)试验,研究 Lirilumab、Nivolumab 单用或与 AZA 联合应用对 MDS 患者的治疗作用。
ASCO 2018 年会,MD 安德森癌症中心将带来关于该项试验的最新进展[4]。截至目前,试验一共入组 10 名 MDS 患者(2 名低风险、8 名高风险患者)。MDS 低风险患者每 4 周接受一次Lirilumab (3mg/kg) 治疗;高风险患者,接受 1-7 天 AZA(75mg/m2)+第 7 天Lirilumab (3mg/kg)治疗。治疗前,10 名患者均接受下一代基因组测序,检测到的突变基因包括 TP53(n=5)、TET2(n=3)、NRAS(n=2)。
治疗后,2 名患者达到完全响应,5 名患者达到骨髓完全响应,3 名患者疾病稳定。研究终止的原因包括疾病进展(n=4)、干细胞移植(n=3)、非治疗相关毒性(n=1)。完全响应/骨髓完全响应的中位持续时间为 3 个月。3/4 级不良反应包括中性粒细胞减少性感染(n=3)、肺炎(n=2)、感染性肠炎(n=1)、胆红素升高(n=1)。研究结果表明,Lirilumab 单用或与 AZA 联用在 MDS 患者中耐受良好。
3.KIR作为肿瘤免疫治疗生物标志物(摘要号:7008,临床试验号:NCT01787474;摘要号:8006,临床试验号:NCT01729091)
由于抑制性 KIR 受体与 HLA 分子之间的相互作用会抑制 NK 细胞的激活和抗肿瘤作用,利用 NK 细胞进行肿瘤免疫治疗常常将 NK 细胞的 KIR 作为一种生物标志物。
一项 phase 1 试验(NCT01787474)[5]将体外扩增的 NK 细胞输送给复发性/难治性髓细胞白血病患者。供体的 NK 细胞经过 KIR 配体筛选或 KIR 基因定量,筛选出最低限度 KIR 表达的 NK 细胞。13 名患者经过 G-CSF、氟达拉滨(Fludarabine)、阿糖胞苷(Cytarabine)治疗后,接受 NK 细胞输注。
11 名可评估患者中,总体骨髓缓解率(overall marrow remission rate)达到 85%。
由于免疫系统紊乱或衰竭,多发性骨髓瘤的一种治疗方法是用化疗方法清除患者体内所有的免疫细胞,然后用健康供体的干细胞回输给肿瘤患者,重建患者的免疫系统。一项 phase 2 试验(NCT01729091)[6]在干细胞移植的基础上,将体外扩增的脐带血 NK 细胞用于多发性骨髓瘤的治疗。
配型过程中,优先 NK 细胞 KIR-HLA 不匹配(mismatch),以降低患者自身对供体 NK 细胞的抑制。33 名患者中,3 个月完全响应率(CR)为 55%(18/33)、较好部分反应率(VGPR)为 12%(4/33)、部分响应率(PR)为 21%(7/33)。然而,22 个月时,10 名患者出现疾病进展,3 名患者死亡,中位疾病无进展存活期(median PFS)未达预期。
以上两项研究表明,利用 NK 细胞作为肿瘤免疫治疗手段时,供体 NK 细胞的 KIR 与患者 HLA 分子不匹配已经成为一种日常实践。有的研究(NCT00748319)直接研究不同的 KIR 受体表达量与皮肤性 T 细胞淋巴癌愈后的相关关系,而 NK 细胞 KIR 基因型检测也已经商业化 (Linkage Biosciences, LinkSeq PCR KIR genotyping)。
3
结言
NK 细胞 KIR 靶点是肿瘤免疫治疗中“年龄较小”的靶点,2007 年 Innate Pharma 的第一个靶向 KIR 单抗 IPH2101 (1-7F9)才步入临床,截至目前,直接靶向 KIR 的产品仅有 Lirilumab (IPH2102)、IPH4102 两个,且均来自 Innate Pharma 一家公司。
在中国,2012 年因内特制药股份有限公司针对 KIR,申请 anti-KIR 单抗专利,治疗发炎及自体免疫疾病。此靶点在中国的关注度较低,也没有相关药企开展对这个靶点的研发计划的报道。以 KIR 为靶点的研究仍处于空间大、低竞争阶段。
此外,将 KIR 作为免疫治疗生物标志物的研究表明,除了直接靶向 KIR,在研的 NK 细胞产品 (CAR-NK, bispecific-linker NK)应考虑降低其 NK 细胞产品的 KIR 表达量或者优先 KIR-HLA mismatch,以期提高自身 NK 细胞的抗肿瘤活性。
关于这一理论概念的实践,请关注美柏医健 PD-(L)1联合疗法专题中针对 KIR 靶点的深度分析系列文章。
参考文献
- PD-(L)1联合疗法专题
- DOI: https://doi.org/10.1016/j.jtho.2017.10.011. Journal of Thoracic Onclogy, 13(1): 106-111.
- JClin Oncol 36, 2018 (suppl; abstr 6015)
- JClin Oncol 36, 2018 (suppl; abstr 7067)
- JClin Oncol 36, 2018 (suppl; abstr 7008)
- JClin Oncol 36, 2018 (suppl; abstr 8006)
- DOI:10.1200/JCO.2017.35.15_suppl.9084. Journal of clinical Oncology 35,no. 15_suppl (May 20 2017) 9084-9084.


本期作者:Echo 徐
北京大学药学院本硕,现约翰霍普金斯大学在读博士,研究免疫代谢、肿瘤免疫相关课题。
精选内容
美柏路演
▼ 点击阅读原文,查看更多好内容
阅读原文 最新评论
推荐文章
作者最新文章
你可能感兴趣的文章
Copyright Disclaimer: The copyright of contents (including texts, images, videos and audios) posted above belong to the User who shared or the third-party website which the User shared from. If you found your copyright have been infringed, please send a DMCA takedown notice to [email protected]. For more detail of the source, please click on the button "Read Original Post" below. For other communications, please send to [email protected].
版权声明:以上内容为用户推荐收藏至CareerEngine平台,其内容(含文字、图片、视频、音频等)及知识版权均属用户或用户转发自的第三方网站,如涉嫌侵权,请通知[email protected]进行信息删除。如需查看信息来源,请点击“查看原文”。如需洽谈其它事宜,请联系[email protected]。
版权声明:以上内容为用户推荐收藏至CareerEngine平台,其内容(含文字、图片、视频、音频等)及知识版权均属用户或用户转发自的第三方网站,如涉嫌侵权,请通知[email protected]进行信息删除。如需查看信息来源,请点击“查看原文”。如需洽谈其它事宜,请联系[email protected]。